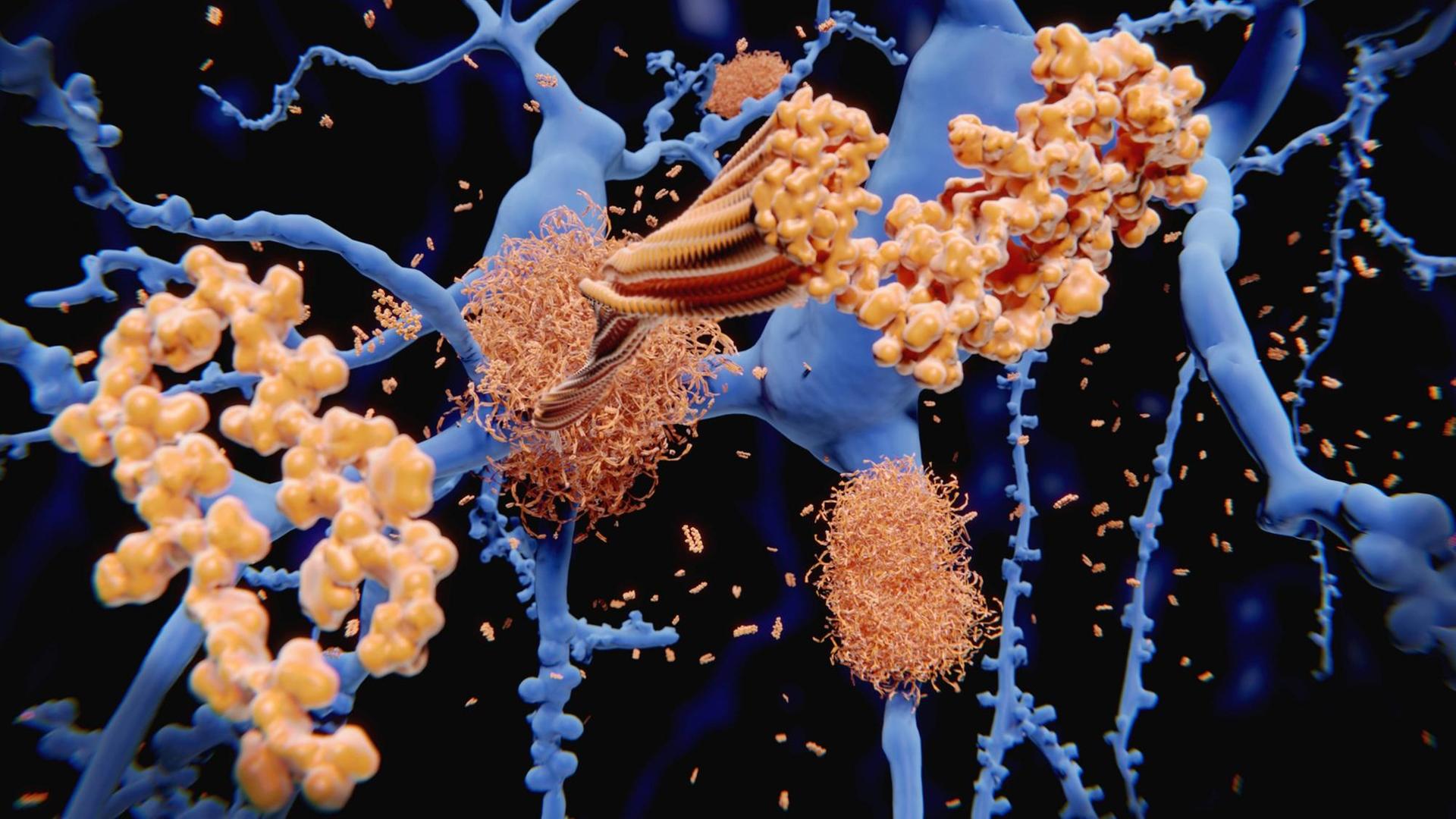
Die degenerativen Prozesse bei Alzheimer sind seit langem bekannt: Im Gehirn der Betroffenen sammeln sich giftige Eiweißklumpen an, die die Nervenzellen schädigen. Aber trotz intensiver Forschung gibt es bislang keine Therapie für die Erkrankung: Ein Wirkstoff-Hoffnungsträger nach dem anderen scheitert, viele Firmen steigen aus der Forschung nach Alzheimer-Medikamenten aus.
Im Frühjahr 2019 werden zwei Studien mit dem als vielversprechend geltenden Antikörper Aducanumab gestoppt und als Fehlschlag eingestuft. Im Herbst 2019 dann die Kehrtwende: Eine neue Analyse der Studienergebnisse habe ein positives Ergebnis für die Studie ergeben - so die US-Firma Biogen. Das Unternehmen plant nun für 2020 einen Zulassungsantrag für Aducanumab bei der US-Gesundheitsbehörde FDA.
"Ein wichtiges Jahr für die Alzheimer-Forschung"
Die Diskussion um Aducanumab habe viele neue Erkenntnisse gebracht, so sieht es Prof. Dr. Michael Heneka, Direktor der Klinik für Neurodegenerative Erkrankungen und Gerontopsychiatrie der Universität Bonn. Die beiden Studien seien zeitlich nicht exakt parallel verlaufen, beim Zeitpunkt der Auswertung habe es eine "asymmetrische Datenlage" gegeben.
"Als der gesamte Datensatz der Studie vorlag, gab sich aber ein anderes Bild. Und es kam dabei heraus, dass die Patienten, die mit der höchsten Dosis für eine lange Zeit behandelt wurden, tatsächlich auch einen leichten positiven Effekt auf die Gedächtnisfunktionen und einen ausgeprägten Effekt auf den Abbau der Beta-Amyloid-Eiweiße aus dem Gehirn gezeigt hatten."

Antikörper hilft Immunzellen beim Eiweiß-Abbau
Der Wirkmechanismus von Aducanumab sei weitgehend aufgeklärt, so Heneka: "Da geht man davon aus, dass die Immunzellen des Gehirns, die Mikrogliazellen, das Amyloid besser abbauen können, wenn es Antikörper-gebunden ist."
Die Geschichte der Alzheimer-Forschung
1907 beschrieb der Neuropathologe Alois Alzheimer in seiner Veröffentlichung "Über eine eigenartige Erkrankung der Hirnrinde" degenerative Veränderungen im Gehirn einer dementen Patientin - seine Schlussfolgerung: Die "Verwirrtheit" hatte eine biologische Ursache. Danach wird es lange still um die Erkrankung. Erst in den 70er- und 80er-Jahren verstärken sich die Forschungsaktivitäten. Zwei Proteine werden als Beteiligte bei der Krankheitsentstehung identifiziert: Amyloid-ß und das sogenannte Tau-Protein. Aber die Forscher sind uneins, welches Protein bei Alzheimer der Hauptverantwortliche ist.
Das Rätsel des Vergessens: Die Geschichte der Alzheimer-Forschung (04:19) Ein Beitrag von Lukas Kohlenbach
1907 beschrieb der Neuropathologe Alois Alzheimer in seiner Veröffentlichung "Über eine eigenartige Erkrankung der Hirnrinde" degenerative Veränderungen im Gehirn einer dementen Patientin - seine Schlussfolgerung: Die "Verwirrtheit" hatte eine biologische Ursache. Danach wird es lange still um die Erkrankung. Erst in den 70er- und 80er-Jahren verstärken sich die Forschungsaktivitäten. Zwei Proteine werden als Beteiligte bei der Krankheitsentstehung identifiziert: Amyloid-ß und das sogenannte Tau-Protein. Aber die Forscher sind uneins, welches Protein bei Alzheimer der Hauptverantwortliche ist.
Das Rätsel des Vergessens: Die Geschichte der Alzheimer-Forschung (04:19) Ein Beitrag von Lukas Kohlenbach
Auch Prof. Heneka sieht Amyloid in einer zentralen Rolle bei der Alzheimer-Entstehung. Dass seit Ende der 90er Jahre trotzdem so viele gegen Amyloid gerichtete Wirkstoffe in klinischen Tests gescheitert sind, könne daran liegen, dass die Patienten viel zu spät behandelt worden seien: "Wenn Kurzzeitgedächtnis-Defizite bestehen und wenn weitere kognitive Domänen beeinträchtigt sind, dann ist die Hirnschädigung so ausgeprägt, dass es wahrscheinlich für viele der therapeutischen Ansätze hinter dem 'Point of no return' ist, und mit dem Amyloid-Ansatz zu diesem Zeitpunkt wahrscheinlich kein wirklich wirksamer krankheitsverzögerter Effekt mehr erreicht werden kann."
Die teure Suche nach dem "Blockbuster-Medikament"
Ein wirksames Therapeutikum gegen Alzheimer zu entwickeln, verspräche vermutlich gewaltige Profite für den Hersteller - andererseits liegen die Kosten für eine große Pharmastudie im dreistelligen Millionenbereich. Heneka sieht die unklaren Erfolgsaussichten als einen möglichen Grund für den Rückzug vieler Pharmafirmen aus der Alzheimerforschung: "Ich glaube, dass es diesen Blockbuster oder dieses einzelne Medikament nie geben wird." Man könne sich die Alzheimerkrankheit wie einen Staffellauf vorstellen, bei dem unterschiedlichste Mechanismen ineinander griffen. "Und das bedingt dann, dass wir nicht mit einem Medikament weiterkommen, sondern wahrscheinlich Kombinationspräparate brauchen, die an unterschiedlichen Stellen angreifen, um letztendlich einen maximal verlaufsverzögernden oder präventiven Effekt zu erzielen."
Die Zukunft der Alzheimer-Forschung
Ob Aducanumab letztlich eine Zulassung für den klinischen Einsatz bekommt, bleibt abzuwarten. Möglicherweise sind aber Antikörper-Wirkstoffe letztlich doch eine Sackgasse - Forscher arbeiten auch an alternativen Ansätzen, etwa an Enzymen, welche die giftigen Eiweiße abbauen könnten. Offenbar stehen Amyloid-ß- und Tau-Stoffwechsel in Zusammenhang - das erschwert die Suche nach einem "Patent-Wirkstoff".
Das Rätsel des Vergessens: Zukunft der Alzheimer-Forschung (04:47) Ein Beitrag von Lukas Kohlenbach
Ob Aducanumab letztlich eine Zulassung für den klinischen Einsatz bekommt, bleibt abzuwarten. Möglicherweise sind aber Antikörper-Wirkstoffe letztlich doch eine Sackgasse - Forscher arbeiten auch an alternativen Ansätzen, etwa an Enzymen, welche die giftigen Eiweiße abbauen könnten. Offenbar stehen Amyloid-ß- und Tau-Stoffwechsel in Zusammenhang - das erschwert die Suche nach einem "Patent-Wirkstoff".
Das Rätsel des Vergessens: Zukunft der Alzheimer-Forschung (04:47) Ein Beitrag von Lukas Kohlenbach
Genetische Abläufe besser verstehen
Den einen "Königsweg" sieht Michael Heneka auch bei alternativen Therapie-Ansätzen nicht; möglicherweise müsse man sich "sehr präzise jeden einzelnen Patienten" ansehen und jeweils die gerade führenden Krankheitsmechanismen identifizieren, um dann einen entsprechenden Wirkstoffcocktail dosieren zu können. Für vielversprechend hält Heneka die in letzten Jahren neu gewonnenen Einsichten in die genetischen Abläufe, die bei der Krankheit eine Rolle spielen - von der Proteincodierung bis hin zu angeborenen Immunitätsmechanismen im Gehirn. Aber auch für Ideen wie die elektrische Stimulation von Nervenzellen müsse man "maximal offen sein, um sie einer genauen klinischen Prüfung zu unterziehen wie auch jedes Medikament."


