
Die Lüftung rauscht laut, Wände und Decke sind komplett mit Kupfer ausgekleidet. Es ist ein ungewöhnlicher Raum, den Tobias Knopp gerade betreten hat. Die rötlich schimmernden Metallwände haben einen konkreten Zweck, sagt der Professor für Biomedizinische Bildgebung am UKE in Hamburg.
"Der Grund ist, dass Kupfer keine Störsignale macht. Wenn man außen magnetisches Material hätte hinter der Kupferwand, können diese Störsignale nicht durch das Kupfer durchkommen."
Die Abschirmung schützt den hochsensiblen Apparat in der Mitte des Raums vor Störfeldern von außen. Auf den ersten Blick sieht er aus wie ein MRT-Scanner, wie man ihn heute in jedem Krankenhaus findet.
"Bloß die Röhre ist kleiner. Die ist zwölf Zentimeter im Durchmesser. Man kann ein kleines Kaninchen oder Mäuse rein tun."
Das Gerät ist ein MPI-Scanner. MPI steht für Magnetic Particle Imaging, auf deutsch: Bildgebung mit magnetischen Partikeln. Ein noch experimentelles Diagnoseverfahren, dessen Grundlagen der Medizintechnik-Konzern Philips im Jahr 2001 erfunden hatte. Präzise Bilder aus dem Körperinneren und genauere Diagnosen erhoffte man sich damals. 2005 war ein Labor-Prototyp fertig, 2009 wurden erste Aufnahmen von den Blutgefäßen einer Maus präsentiert. Seit Kurzem gibt es den MPI-Scanner als kommerzielles Gerät, als Kleintier-Scanner für die Forschung. Mit ihm wollen Tobias Knopp und seine Kollegen herausfinden, ob MPI hält, was es verspricht. Basis der Methode ist ein Kontrastmittel, das in den Körper injiziert wird und auf Magnetfelder anspricht.
"Das sind kleine Eisenoxid-Partikel. Im Prinzip ist das die gleiche Zusammensetzung wie Rost. Es ist so, dass diese Partikel überhaupt nicht schädlich sind für den Menschen. Die werden einfach wieder abgebaut."
Im Körper reagieren die Rostpartikel sehr empfindlich auf das Magnetfeld des Scanners und fangen an zu schwingen. Diese Schwingungen lassen sich durch Sensoren messen, eine Software setzt deren Signale zu einem Bild zusammen.
"Das Schöne an MPI ist, dass man nur das Kontrastmittel sieht. Wenn sich das Kontrastmittel entlang der Blutbahn bewegt, sieht man zum Beispiel wirklich schön das Herz schlagen."

Heute wollen die Forscher mit ihrem Scanner eine Maus untersuchen.
"Jetzt muss ich aufpassen. Tür auf! Die darf nicht wegrutschen!"
Behutsam hat UKE-Physiker Michael Kaul die schlafende Maus in einen dünnen Kunststoffzylinder gebettet. Auf der Mäusenase sitzt eine winzige Atemmaske, durch die das Narkosemittel strömt. Dann schiebt Kaul den Zylinder in die Röhre des Scanners.
"Das ist alles in Ordnung. Jetzt können wir die Spritze mit dem Kontrastmittel umsetzen und unsere Bildgebung starten."
- "Finger weg!"
Kaul schließt die massive Tür zum Untersuchungsraum.
"Sind jetzt startklar. Und ich aktiviere genau jetzt."
Etwas später erscheint auf dem Rechner ein erstes Bild. Skeptisch schaut es sich Michael Kaul an.
"Jetzt sehen wir hier einen hellen Punkt. Aber ich weiß nicht - das ist, glaube ich, nichts."
Bald ist die Ursache gefunden, ein Messparameter war falsch eingestellt. Der Physiker muss die Messung wiederholen - diesmal mit mehr Erfolg.
"Man sieht hier große Gefäße. Und in den Gefäßen und drum herum leuchtet es. Weil das das Signal ist, was das MPI liefert."
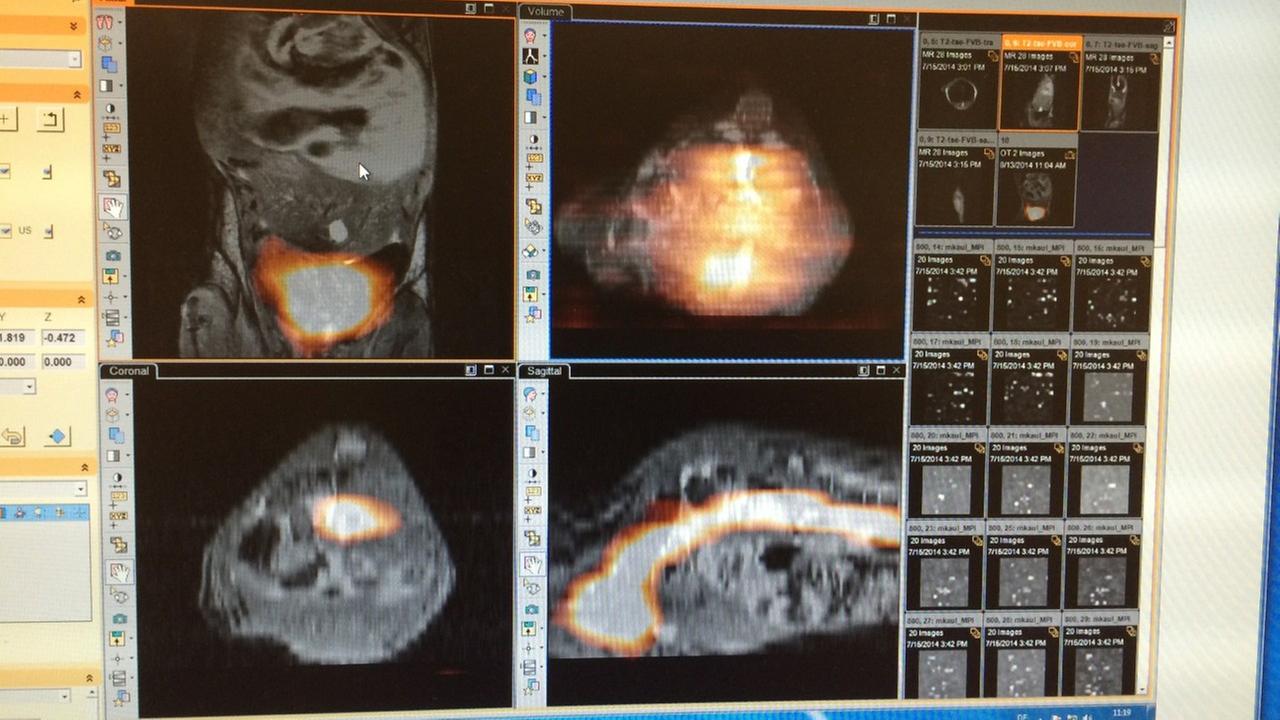
Das Bild ist eine Überlagerung zweier Aufnahmen: Ein zuvor gemachtes MRT-Bild zeigt schemenhaft die Organe der Maus. Darüber gelegt sind die hellen Leuchtspuren aus dem MPI-Scanner. Sie heben die Blutgefäße deutlich heraus. Michael Kaul ist zufrieden:
"Hier ist das interessant, dass hier das Herz ist. Und vom Herzen ausgehend verläuft die Vena cava durch die Leber."
Und was genau erhoffen sich die Mediziner von dem neuen Verfahren?
"Das Potenzial von MPI deutet darauf hin, dass es erstens empfindlicher und zweitens wesentlich schneller als die bisher etablierten bildgebenden Verfahren ist", sagt Professor Gerhard Adam, Leiter der Radiologie am UKE. Gefäßerkrankungen könnten sich mit MPI besser diagnostizieren lassen, aber auch Tumoren im Frühstadium, so Adams Kollege Harald Ittrich:
"Da dringt man in den Bereich der Nanomedizin ein. Man könnte sich vorstellen, diese Eisenoxid-Partikel spezifisch bindend zu machen, sodass sie an spezifische Oberflächen von Tumoren binden. Und einem dann verraten, wie der Tumor beschaffen ist, worauf er reagieren könnte, um ihn besser therapieren zu können."
Zuvor aber ist noch manche Herausforderung zu meistern. Denn bislang ist noch gar nicht bewiesen, dass die MPI-Bilder tatsächlich einen diagnostischen Mehrwert bringen, insbesondere im Vergleich zu MRT-Scannern. Die nämlich sind in den letzten Jahren immer leistungsfähiger geworden. Ein weiteres Problem: Noch braucht es zu viel Kontrastmittel, damit das Verfahren funktioniert. Ittrich:
"Man kann die Nanopartikel später nicht in unbegrenzten Dosen in Patienten spritzen. Insofern muss daran gearbeitet werden, das Verfahren dahin zu trimmen, kleine Mengen dieser Partikel abzubilden. Da kann man sowohl an der Maschine entwickeln, aber auch von der Kontrastmittel-Seite einiges auf die Beine stellen."
Probleme, die nicht nur die Hamburger mit ihrem Kleintierscanner in den Griff bekommen wollen. Auch anderswo wird an der Methode getüftelt, etwa an der Charité in Berlin, sagt Adam:
"Wir hoffen, in vier bis fünf Jahren einen Scanner in Betrieb nehmen zu können, auf dem wir dann die experimentellen Ergebnisse, die wir gesammelt haben, in eine humane Anwendung bringen können. Wir sind optimistisch, dass was draus wird."
Zwar ist es schon fast 15 Jahre her, dass Philips die Grundzüge der neuen Methode entwickelte. Doch die Nagelprobe, also die Erprobung des neuen Verfahrens am Menschen, wird wohl noch eine Weile auf sich warten lassen.
