Es ist Mittag. Dirk Trauner hat sein Büro verlassen. Er steht auf der Straße, blickt zum hellblauen Himmel hoch, zur Sonne. Licht spielt für die Forschung des Biochemikers eine wichtige Rolle.
"Wir versuchen, mithilfe von fotoschaltbaren Molekülen das Licht auszunützen, um damit Biologie zu betreiben, um damit biologische Prozesse sehr präzise steuern zu können."
Der Professor für chemische Biologie und Genetik entwickelt an der Ludwig-Maximilians-Universität München Arzneistoffe, die sich mithilfe von Licht aktivieren lassen. Dirk Trauner macht sozusagen blinde Moleküle sehend, indem er eine Art photochemischen Schalter in sie einbaut. Dessen Gestalt lässt sich durch Licht einer bestimmten Wellenlänge ändern. Blaues Licht klappt den lang gestreckten Schalter um zu einer angewinkelten Form, und grünes Licht kehrt den Vorgang wieder um. Und damit ahmt der Forscher ein Prinzip nach, das so ähnlich auch in der Natur vorkommt.
"Zum Beispiel im Sehprozess, im natürlichen, menschlichen Sehprozess. Es gibt aber auch synthetische Moleküle, die genau dasselbe machen."
Solche synthetischen Molekülschalter bauen Dirk Trauner und seine Mitarbeiter in Moleküle ein, die im menschlichen Körper eine bestimmte Funktion erfüllen.
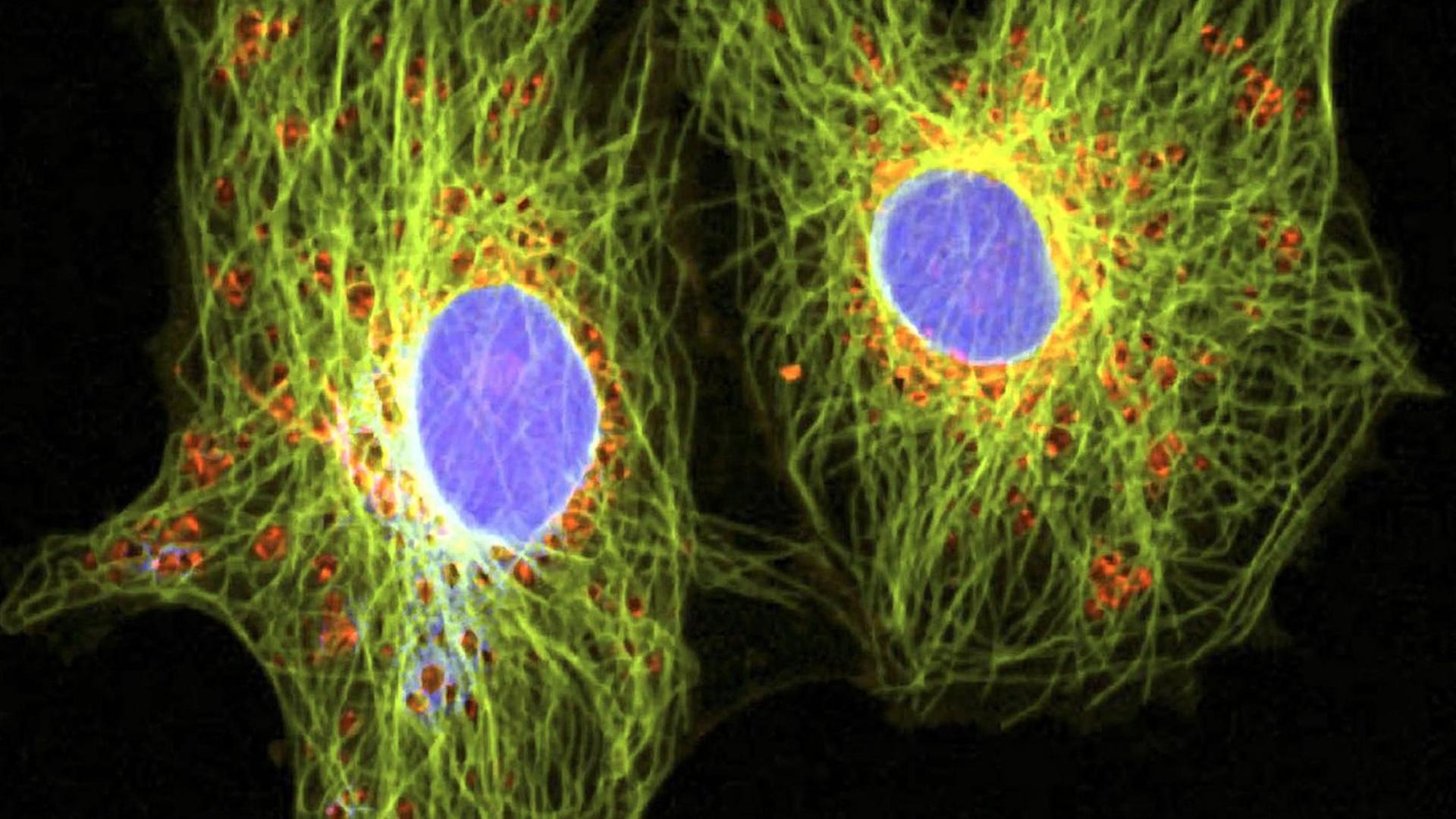
"Zum Beispiel die Proteine, die für das Feuern von Nervenzellen verantwortlich sind. Oder die Proteine, die für die Bewegung von Zellen verantwortlich sind, für die Teilung von Zellen. Die können wir jetzt lichtempfindlich machen und mit Licht an- und ausschalten. Und das eröffnet natürlich große Möglichkeiten in der Neurobiologie und in der Zellbiologie und möglicherweise sogar in der Krebstherapie."
Für die Krebstherapie hat der Biochemiker sogenannte Photostatine entwickelt. Chemisch ähneln sie dem Colchicin. Das ist das Pflanzengift aus der Herbstzeitlosen. In der Vergangenheit wurde bereits versucht, mit dieser Substanz Tumorzellen zu bekämpfen, denn sie behindert die Zellteilung – die Versuche blieben jedoch erfolglos.
"Obwohl es ein sehr wirksames Molekül ist, kann es in der Krebstherapie nicht eingesetzt werden, da es zu toxisch ist."
Colchicin verhindert, dass sich bei der Zellteilung die sogenannten Spindelfasern bilden. Die teilen das Erbgut der Zelle gleichmäßig auf die beiden Tochterzellen auf. Wird dieser Prozess durch das Zellgift gestört, dann sterben die Tochterzellen ab. Im Tumorgewebe ist das natürlich erwünscht.
"Aber eben nur in Krebs und nicht sonst wo. Und Sie wollen das nicht machen zum Beispiel irgendwo im Darmepithel, an ihren Haarzellen. Diese Nebenwirkungen haben Sie ja, wenn Sie gewisse Krebsmedikamente nehmen. Und unser Ziel ist jetzt, dieses Zellgift so umzubauen, dass es nur dort giftig wird, wo es beleuchtet wird. Das ist uns gelungen mit den Photostatinen."
Das synthetische Molekül wird mit blauem Licht im Tumorgewebe aktiviert. Das Besondere an der Substanz: Der Molekülschalter klappt von alleine wieder zurück, wenn er nicht mehr bestrahlt wird.
"Sobald die Verbindung aus dem Licht raus diffundiert oder raus geschwemmt wird, würde sie in eine inaktive, nicht toxische Dunkelform wiederum umklappen."
Damit ließen sich Krebsarten bekämpfen, die zum Beispiel mit LEDs gut zu erreichen sind. Der Münchner Forscher denkt etwa an Karzinome im Darm oder der Blase. Dirk Trauner gibt jedoch auch zu bedenken, dass solch eine Therapie noch etwas auf sich warten lassen dürfte.
"Bisher ist das alles nur auf Zellebene, auf der Ebene von einfachen Versuchstieren wie zum Beispiel C. Elegans, Wurmembryos, gelungen. Der Sprung zum Mensch ist sicher ein sehr großer und wird viele Jahre dauern. Aber wir glauben daran, dass dieses Konzept im Prinzip schlüssig ist und dass es hoffentlich eines Tages auch im Menschen angewendet wird."