Bakterien, Viren, Parasiten: Der Mensch lebt in einer Welt voller Mikroben, mit den meisten hat er sich arrangiert. Auch Pilze haben den Menschen bislang kaum behelligt. Doch das muss nicht so bleiben.
„Bei Candida auris sind wir beunruhigt, weil er der erste Erreger sein könnte, der die Temperaturbarriere durchbrochen hat. Ich werde Ihnen erzählen, warum", sagt Arturo Casadevall. Er ist Mikrobiologe und forscht an der Johns Hopkins School of Public Health in Baltimore. „Die meisten Menschen machen sich wegen Pilzkrankheiten keine Sorgen. Höchstens, wenn sie mal einen Nagelpilz haben. Wir haben zwar Angst vor Viren, Malaria oder Tuberkulosebakterien, aber nicht vor Pilzen."
Diese Sendung wurde erstmals am 5.6.2022 ausgestrahlt.
Dabei sei ihre Zerstörungskraft gewaltig. "Überall auf der Welt bringen sie ganze Tier- und Pflanzenpopulationen an den Rand der Existenz", sagt Constantin Urban, Immunologe an der Umeå Universität in Schweden: „Im Tierreich sehen wir das ja schon. Es gibt eben diese Chytridpilze, die Amphibien, vor allem Frösche infizieren können und einfach zu Massenaussterben und auch schon zur Auslöschung bestimmter Froscharten geführt hat.“
„Viele Tiere kriegen ganz viele Pilzinfektionen", sagt auch Oliver Kurzai, Vorstand des Instituts für Hygiene und Mikrobiologie am Universitätsklinikum Würzburg. "Pflanzen kriegen ganz viele Pilzinfektionen. Tatsächlich führt eigentlich, wenn ich es ökologisch betrachte, kein Infektionserreger so häufig zu Artensterben wie die Pilze.“
Immunsystem wird normalerweise mit Pilzen fertig
Säugetiere wie den Menschen dagegen greifen sie nur dann an, wenn deren Immunsystem geschwächt ist. „Tatsächlich können sich Pilze anpassen, und wir sehen gerade in letzter Zeit auch Veränderungen und neue Erreger, die zum Beispiel als Infektionserreger auftreten, die wir vorher gar nicht so gesehen haben.“
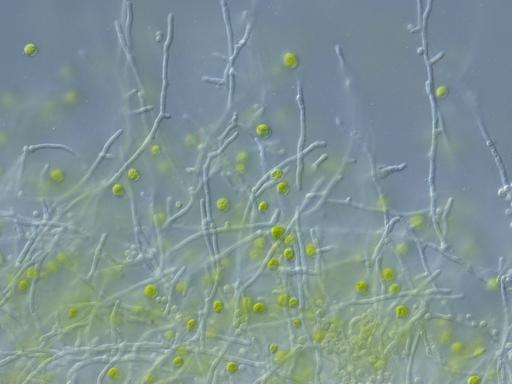
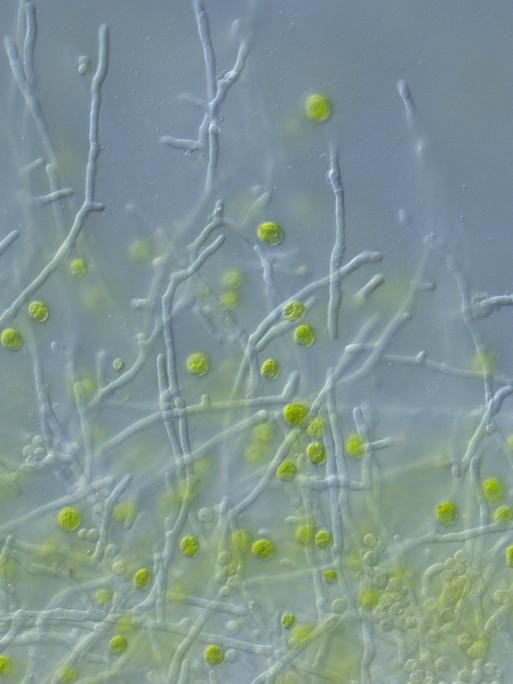
In jedem Kubikmeter Luft schweben zwischen 1.000 und 10.000 Pilzsporen. Tagtäglich atmen wir unzählige davon ein. Krank machen sie uns nicht. An den Eintrittspforten in den Körper, wie zum Beispiel der Lunge, verstellen ihnen Immunzellen den Weg. „Unser Immunsystem ist wirklich exzellent in der Lage, Pilze zu bekämpfen. Da gibt es bestimmte Bestandteile, zum Beispiel bestimmte Zellen im Blut, die wirklich Pilze sehr effizient angreifen und töten. Das schützt uns eigentlich vor solchen lebensbedrohlichen Infektionen.“
Doch allein in Deutschland leben Schätzungen zufolge etwa vier Millionen Menschen mit eingeschränkter Abwehr. „Diese Patienten, die sind tatsächlich in den letzten Jahrzehnten, so ich würde denken ab den 70er-, 80er-Jahren wesentlich häufiger geworden. Dann müssen Sie einfach mal denken an die Entwicklung der modernen Medizin: Organtransplantation, Stammzelltransplantation, ab den 80er-Jahren die HIV-Pandemie. All das hat dazu geführt, dass wirklich diese immunsupprimierten Patienten, also Patienten, deren Immunsystem nicht mehr richtig funktioniert, zugenommen haben, und diese Patienten kriegen invasive Pilzinfektionen.“
Plötzlich infizieren sich Covid-Patienten in Indien mit dem Schwarzen Pilz
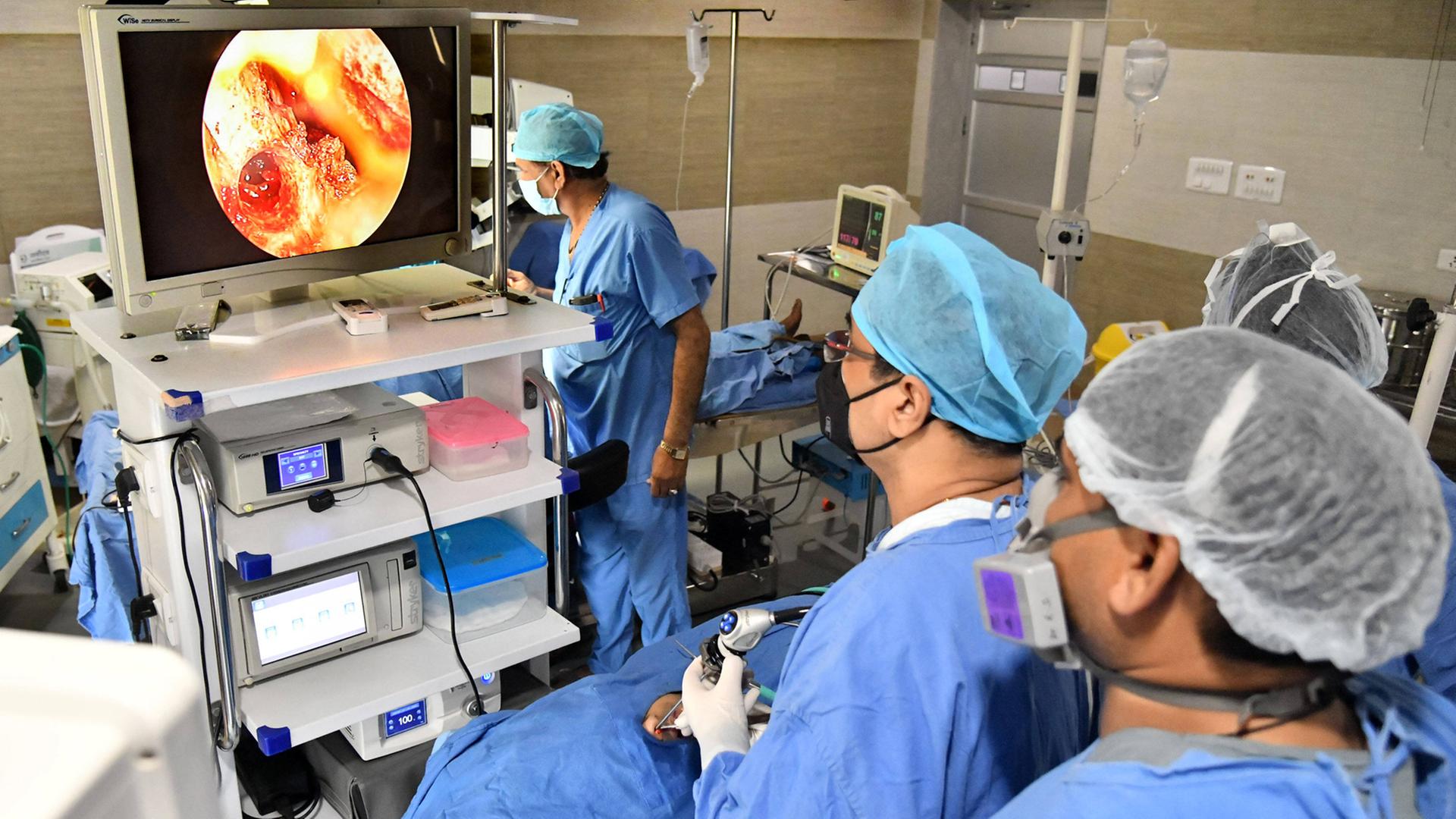
Wie angreifbar Menschen werden, wenn ihr Immunsystem sie nicht mehr schützt, hat sich im Mai 2021 in Indien gezeigt. Damals erreicht die Covidpandemie dort einen neuen Höhepunkt. Die Krankenhäuser sind überfüllt, viele Patienten müssen beatmet werden. Dann greift eine neue Krankheit um sich. Ein Fernsehbericht: “Der Schwarze Pilz hat den Patienten längst befallen, greift Organe an, frisst sich durch das Gewebe. Agressiv! Jeder zweite stirbt daran.”
Dramatische Bilder gingen um die Welt. Sie zeigen Menschen mit schwarz gefärbten Nasen, die Augen von einer dicken schwarzen Kruste bedeckt. Um die Patienten zu retten, müssen ÄrztInnen das befallene Gewebe entfernen. Wo der Pilz in den Körper gelangt, löst er eine Blutvergiftung aus. Jeder zweite stirbt an der Infektion.
"Ich habe so etwas noch nie erlebt"
Allein im indischen Bundesstaat Maharashtra sind es mehr als 1.200 Tote. Eine Ausnahmesituation, sagt Oliver Kurzai. „Ich habe sowas noch nie erlebt. Ich habe eine Kollegin aus Indien gesprochen, die gesagt hat, dass eigene Stationen in den Krankenhäusern eingerichtet worden sind, nur um diese Patienten zu behandeln. Diese Patienten brauchen häufig eine operative Therapie. Da muss ein Teil des infizierten Gewebes weggeschnitten werden, und es gab OP-Pläne, die den ganzen Tag nur einen Patienten mit Pilzinfektion nach dem anderen auf dem OP-Plan hatten. Das ist unglaublich dramatisch gewesen, wegen extrem hoher Covid-Zahlen, zusätzlich einer sehr freizügigen Therapie mit Cortison, die prinzipiell natürlich sinnvoll ist bei diesen Patienten, aber nicht in einer unkontrollierten Dosierung, die dann zu einer schweren Immunsuppression führt, und einer sehr hohen Rate von Patienten, die zuckerkrank sind.“
Das Cortison hat nicht nur die überschießende Immunreaktion auf das Coronavirus gebremst. Viele der Betroffenen waren Diabetiker. Der hohe Zuckergehalt in ihrem Körper bot den Pilzen optimale Wachstumsbedingungen. „Und diese drei Risikofaktoren zusammen haben wahrscheinlich dazu geführt, dass es diese enormen Zahlen in Indien gab, Tausende von Fällen. Wir haben in Deutschland geguckt, wie viele solcher Infektionen es gab, und die aktuelle Zahl, die ich zuverlässig berichten kann, liegt bei 16, glaube ich. Das hat hier keine Rolle gespielt.“

Die Menschen werden älter - und anfälliger
Eine Zeitenwende bahnt sich an. Diphterie, Pest oder Polio haben ihren Schrecken verloren. Aber auch chronische Krankheiten wie Krebs oder Diabetes sind heutzutage kein Todesurteil mehr. Die Menschen werden immer älter - und damit anfälliger für Infektionskrankheiten. „Wenn Sie einem Arzt aus dem vorigen Jahrhundert zeigen würden, mit welchen Mikroorganismen wir heute Probleme haben, wäre er schockiert", sagt Arturo Casadevall. "Denn diese Mikroben waren damals nicht pathogen."
Einhundert Jahre sind aus evolutionsbiologischer Sicht noch nicht mal ein Wimpernschlag, sagt Casadevall. „Vor hundert Jahren hatten alle Menschen entweder ein funktionierendes Immunsystem - oder sie sind gestorben. Es gab deshalb nicht viele Menschen mit eingeschränkter Immunabwehr. Heute haben wir es bei den Infektionskrankheiten mit ganz anderen Problemen zu tun. Im Wesentlichen, weil wir den menschlichen Wirt verändert haben.“
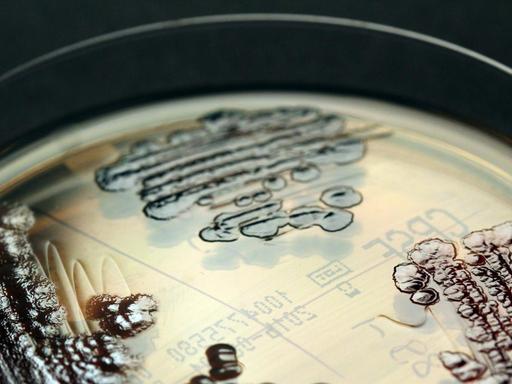
Auf den Intensivstationen dieser Welt überleben Menschen, deren Immunsystem kaum noch in der Lage ist, sich gegen Keime zur Wehr zu setzen. Erste Pilze haben gelernt, diese Schlupflöcher der menschlichen Abwehr zu nutzen, und es tauchen neue Erreger auf. Candida auris zum Beispiel. 2009 entdeckten Ärzte diesen Pilz im Ohr einer chinesischen Patientin. "‚Auris‘, lateinisch für Ohr, so hat man das dann genannt", sagt Oliver Kurzai, "und dann hat man in den nächsten Jahren gemerkt, dass dieser Pilz plötzlich an anderen Stellen der Welt auch auftritt.“

Ein neuer, gefährlicher Erreger taucht auf
Inzwischen sind weltweit mehrere hundert Menschen an Candida auris gestorben. „Der Pilz hat dramatisch große Ausbrüche in Krankenhäusern verursacht, zunächst in Asien, in Indien auch, aber dann auch in Südafrika und in Europa, vor allem in England und in Spanien, unglaublich schwer zu kontrollierende krankenhaushygienische Notfallsituationen.“
Eindämmen lässt er sich kaum. Schon jetzt ist er immun gegen viele gängige Antimykotika, mit denen ÄrztInnen Pilzinfektionen behandeln. „Die Resistenzen sind deswegen so problematisch, weil sie häufig Medikamente betreffen, die wir als sogenannte Erstlinientherapie einsetzen, also bevorzugt gegeben werden, weil wir wissen, dass sie am besten wirken. Wenn bei Pilzen diese Erstlinientherapie ausfällt, dann ist die Zweitlinientherapie häufig wesentlich schlechter, weil wir sehr viel weniger Antimykotika haben als Antibiotika, die gegen Bakterien wirken. Diese Kombination: Wenig Option für die Behandlung und zunehmende Resistenzen ist tatsächlich etwas, was einem aus medizinischer Sicht Sorgen machen sollte.“
Und es gibt eine weitere Eigenschaft, die Candida auris gefährlich macht: Er breitet sich von Mensch zu Mensch aus. „Candida auris hat in einigen Ländern, insbesondere in Indien und Südafrika, angefangen, andere Pilze zu verdrängen. Das kann man sich gut vorstellen: Wenn Candida auris sich im Krankenhaus immer wieder verbreitet von Mensch zu Mensch, dann wird er irgendwann häufiger werden, und in diesen Ländern haben wir gesehen, dass die Zahl der Blutstrominfektionen, also der Sepsisfälle, die durch Candida auris verursacht wird, immer weiter zugenommen hat. Dann ersetzen wir natürlich eine womöglich eher sensible Art, die wir vorher hatten, durch eine jetzt resistente Art, die noch dazu im Krankenhaus verbreitet werden kann. Das ist nicht das, was wir uns wünschen sollten. Ganz klar.“
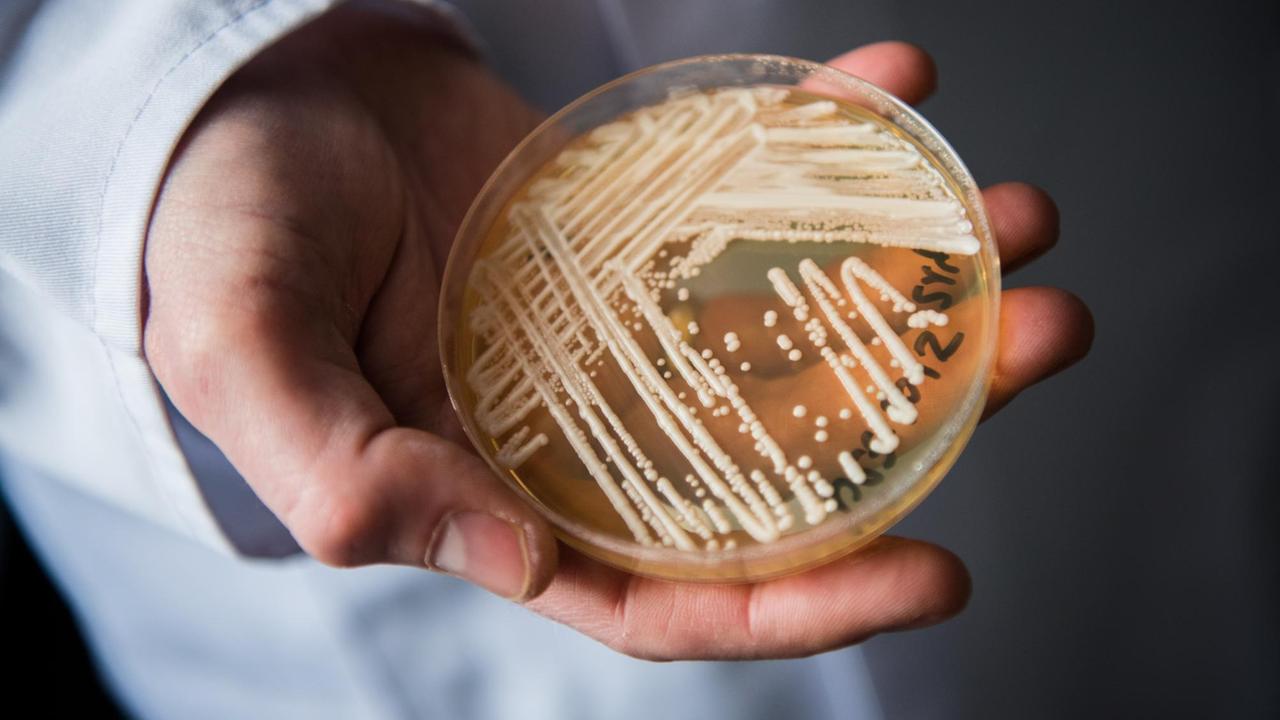
Hat sich Candida auris an unsere Körpertemperatur angepasst?
Candida auris wirft Fragen auf: Wie hat er es geschafft, sich von Mensch zu Mensch auszubreiten? „Die Geschichte ist deswegen so spannend, weil bis heute keiner weiß, wo dieser Pilz herkam. Wie kann es sein, dass er plötzlich ab 2009 überall auf der Welt auftaucht? Woher kommt dieser Pilz? Warum breitet er sich plötzlich so effizient aus?“
Candida auris taucht fast zeitgleich auf drei verschiedenen Kontinenten auf: Afrika, Südamerika, Asien. „Die gefundenen Stämme sind nicht miteinander verwandt", sagt Arturo Casadevall. "Das Ganze ist in einem sehr kurzen Zeitraum passiert, zwischen 2011 und 2012 - und es ist ein Erreger, der in der Medizin vorher komplett unbekannt war.“
Kurz nacheinander waren also an verschiedenen Orten Varianten des Erregers entstanden, die Menschen infizieren konnten. Wo war die Verbindung? Casadevall hat einen Verdacht. „Was haben Südafrika, Venezuela und Indien gemeinsam? Das einzige, das mir einfällt ist: Überall dort wird es wärmer. Anfang des Jahres gab es Berichte, dass Candida auris inzwischen auch auf den indischen Andamanen-Inseln entdeckt wurde. Zwei Isolate an einem Strand, der häufig von Touristen besucht wird. Eine Möglichkeit ist, dass Menschen ihn dort hingebracht haben. Aber ein anderes Isolat wurde in einem Sumpfgebiet entdeckt, weitab von der Zivilisation. Diese Variante ist bei 37 Grad nicht so gut gewachsen, und liefert anekdotische Evidenz für die Theorie, dass sich der Wildtyp von Candida auris ganz allmählich an höhere Temperaturen angepasst hat, bis eine adaptierte Variante entstanden ist, die überleben konnte - und dann taucht sie im Krankenhaus auf.“
37 Grad Celsius - eigentlich zu warm für Pilze
Candida auris könnte der Vorbote einer neuen Generation von Erregern sein. Denn er hat eine Eigenschaft, die ihn von den meisten anderen Pilzen unterscheidet. Er kann die Körpertemperatur des Menschen tolerieren. „So blöd es klingt: 37 Grad ist für die meisten Pilze nicht wahnsinnig angenehm", sagt Oliver Kurza. "Ganz, ganz viele von den über 1,5 Millionen Pilzen, die es wahrscheinlich gibt auf dem Planeten, können bei 37 Grad überhaupt nicht mehr wachsen - und die können uns dann auch nicht infizieren.“
Es gibt Ausnahmen. In unserem Darm leben Pilze mit Bakterien in einer Gemeinschaft. Diese Pilze sind an unsere Temperatur angepasst und es gibt sogar spezielle Immunzellen, die ihnen Zutritt in den Körper gewähren. Doch die meisten anderen Pilze leben im Wald, im Boden, auf Steinen oder in der Biotonne und gedeihen bei molligen 25 Grad am besten. Sie müssten also mehr als zehn Grad überwinden, um auch in uns wachsen zu können.
„Natürlich kann man dann diese Temperatur 37 Grad für Säugetiere als einen Selektionsvorteil sehen, der uns eben begünstigt gegenüber der Verteidigung gegen Pilzinfektionen", bestätigt Constantin Urban.
Säugetiere können ihre Muskeln selbst aufheizen und deshalb auch im Winter jagen. In vielen Lehrbüchern steht, damit seien sie Reptilien überlegen, die bei Kälte zur Bewegungslosigkeit verdammt sind. Dieser Vorteil habe am Ende der Kreidezeit den Siegeszug der Vögel und Säugetiere ermöglicht. Doch was, wenn das noch nicht die ganze Geschichte war?
„Es gibt eben die Theorie, dass mit dem Meteoriteneinschlag, als die Temperatur auf der Erde sank und dann eben die Dinosaurier nicht mehr genug Abwehrkräfte hatten, sich gegen die Pilze zu verteidigen, und die Pilze zumindest mit dazu beigetragen haben, dass die Dinosaurier ausgestorben sind." Die Theorie stammt von Arturo Casadevall selbst.

Dinosaurier mit Pilz-Handicap, Säugetiere im Vorteil?
„Wenn die Leute unsere Story hören, sagen sie: ‚Casadevall sagt, die Pilze haben die Dinosaurier ausgerottet.‘ Nein! Man muss es so sehen: Das Zeitalter der Dinosaurier ging vor 65 Millionen Jahren zu Ende, als die warme Erde durch den Einschlag eines 20, 30 Kilometer langen Meteoriten verwüstet wurde. Er traf Yucatán. Die Dinosaurier starben wahrscheinlich an den Folgen dieser Katastrophe. Es gab damals massive Tsunamis, Stürme und die Erde hat sich abgekühlt. Aber die interessante Frage, die mich immer beschäftigt hat, ist doch: Warum gab es danach kein zweites Zeitalter der Reptilien?“
Die Dinosaurier, die zu den Reptilien gehören, hatten über Millionen von Jahren die Tierwelt dominiert, erzählt der Mikrobiologe von der Johns-Hopkins School für Public Health: „Es folgte das Zeitalter der Säugetiere - Wale, Menschen, Fledermäuse. Die Reptilien spielten nur noch eine untergeordnete Rolle. Was wir vorgeschlagen haben, ist die Idee, dass Pilze damals die Reptilien wie ein Filter draußen hielten. Die Säugetiere waren kleine Kreaturen, sie waren warm, hatten eine hohe Körpertemperatur, sie konnten sich bewegen, sie konnten fressen - und ihre Körpertemperatur schützte sie vor Pilzen. Das könnte erklären, warum wir so resistent sind gegen Pilze.“ Beweisen lässt sich das nicht, gibt Casadevall zu: „Es ist eine Theorie.“
„Ja, das ist natürlich eine schöne Theorie", sagt Constantin Urban, Mikrobiologe in Umea, "aber es verdichten sich ja auch die Kennzeichen, dass Dinosaurier nicht wechselwarm waren, sondern eben auch warmblütig. Ein absolut einschneidendes Beispiel dafür ist, dass man eben Dinosaurier gefunden hat in Australien von der Zeit, wo eben Australien in der Nähe vom Südpol war. Das heißt, da gab es eine dunkle Periode von einem halben Jahr - und in dieser Periode können die Außentemperaturen nicht hoch genug gewesen sein, dass quasi ein wechselwarmes großes Lebewesen überleben kann. Das heißt, wenn jetzt Dinosaurier auch Warmblüter waren, das würde ja im Prinzip dieser Theorie widersprechen, dass sie nur deshalb ausgestorben sind, dass sie alle wechselwarm waren.“
Kompromiss zwischen Schutz und Energieaufwand?
Und Pilze gab es bereits zu Lebzeiten der Dinosaurier. Warum also sollten sie den Riesenechsen das Leben erst nach dem Ende der Kreidezeit schwergemacht haben? Entscheidend könnte die Menge an Pilzen gewesen sein. Dennoch bleibt es eine Korrelation, keine Kausalität. „Wir wissen von geologischen Hinweisen auf ein massives Vorkommen an Pilzsporen am Ende der Kreidezeit", sagt Casadevall, "und wir wissen, dass die Säugetiere damals die Reptilien ersetzt haben.“
Sowohl Säugetiere als auch Vögel haben am Ende der Kreidezeit eine gleichbleibend hohe Körpertemperatur entwickelt. Vor ein paar Jahren hat Casadevall die dafür anfallenden Heizkosten berechnet. Die Energiebilanz deutet auf einen Trade-off hin: einen Kompromiss zwischen Schutz und Energieaufwand.
„Es ist ein indirekter Beweis: Wir haben uns angeschaut, wie gut die Temperatur vor Infektionen schützt und wieviel Energie es kostet, warmblütig zu sein. Wenn man sich dann fragt: Bei welcher Temperatur liegt das Optimum für den besten Schutz, ohne die ganze Zeit fressen zu müssen. Dann sind das 37 Grad. Das legt nahe, dass unsere Temperatur in der Evolution ein Kompromiss war. Wir könnten heißer sein, 40 Grad zum Beispiel, aber dann würden wir sehr viel mehr Kalorien brauchen, um über den Tag zu kommen.“

Weißnasen-Krankheit tötet Fledermäuse im Winterschlaf
Eine Betriebstemperatur von konstanten 37 Grad stellt vor allem kleine Tiere vor Herausforderungen. Manche müssen täglich die Hälfte ihres Körpergewichts an Nahrung aufnehmen, um nicht auszukühlen. Fledermäuse lösen dieses Problem, indem sie ihre Körpertemperatur im Winter auf wenige Grad absenken.
Doch diese Strategie wird zahlreichen Arten in Amerika momentan zum Verhängnis. Seit ein paar Jahren breitet sich dort eine verheerende Seuche unter Fledermausarten aus, die in Höhlen überwintern: die Weißnasen-Krankheit. "Sie wird durch einen Pilz ausgelöst, der aus Europa eingeschleppt wurde. Dort sind die Fledermäuse dagegen immun. Aber in den USA hat der Pilz in den letzten 15 Jahren fast 100 Millionen Tiere umgebracht.“
Erstmals taucht der Erreger 2006 in den USA auf. Fledermausforscher entdecken damals in der Howes Cave im Bundesstaat New York Tausende toter Fledermäuse. Ein weißer Flaum bedeckt die Nasen der Tiere. Es sind die Hyphen des Pilzes Pseudogymnoascus destructans. Seine Sporen waren vermutlich von Touristen eingeschleppt worden, die die Höhlen im Sommer zu Hunderttausenden besuchen. Inzwischen ist der Pilz auch in vielen anderen Höhlen heimisch und hat ganze Fledermauskolonien vernichtet.
Für das Nordamerikanische Mausohr und die Kleine Braune Fledermaus könnte er das Ende bedeuten, sagt Casadevall. „Im Sommer sind die Tiere 37 Grad warm und gegen den Pilz immun. Doch wenn sie überwintern, senken sie ihre Körpertemperatur auf zehn bis zwölf Grad, und dann kann der Pilz in ihnen wachsen und sie töten. Wenn man aber infizierte Fledermäuse ins Labor bringt, ihnen zu fressen gibt und sie dann ihre Körpertemperatur erhöhen, können sie den Pilz abwehren. Das zeigt sehr eindrucksvoll, wie wichtig die Körpertemperatur sein kann, um Pilze fern zu halten.“
Klimawandel "trainiert" Pilze auf Wärme-Toleranz
Dazu passt eine weitere Studie, die Casadevall durchgeführt hat. Für fast 5.000 Pilzstämme hat er bei unterschiedlichen Temperaturen das Wachstum untersucht. 30 Grad tolerierten alle Pilze gut, doch jedes weitere Grad hat ihr Wachstum weiter ausgebremst - und jeweils sechs weitere Prozent der Pilzstämme absterben lassen. Nur ein Bruchteil der Pilzstämme hat jenseits der 37 Grad überlebt.
Damit sind wir für die meisten Pilze eine schwer einzunehmende Festung, Oliver Kurzai: „So ein Schritt zu sagen: Ich schieb mal mein Wachstumsoptimum von 25° zu 37°, da liegen Welten dazwischen.“
Unmöglich ist es aber auch nicht. Pilze sind lebende Organismen. Sie können sich anpassen. „Im Labor ist das machbar", sagt Arturo Casadevall. "Sie können einen Pilz, der nur bis 32 Grad wachsen kann, langsam an höhere Temperaturen gewöhnen. Wir glauben, dass es da draußen Tausende Arten gibt, die beginnen werden, sich anzupassen. Einige von ihnen, nur ganz wenige, werden die nötigen Werkzeuge haben, um sich in uns zu vermehren. Denn Sie erinnern sich: Es geht nicht nur um die Temperatur. Sie müssen auch unsere Immunabwehr besiegen, und die ist wirklich effektiv. Der größte Teil wird das nicht schaffen. Aber einige eben schon - und das ist unsere große Sorge.“
Schon jetzt haben erste Pilze dazugelernt. Der Klimawandel trainiere sie auf höhere Temperaturen, befürchtet Casadevall. „Wir sollten nicht nur auf die Durchschnittstemperatur schauen. Die ist ja bisher nur um etwa ein Grad angestiegen. Was wir uns anschauen müssen, ist die Zahl der Tage mit extremer Hitze. Denn jeder einzelne von ihnen verursacht einen Selektionsdruck, den Organismen überleben müssen. Es ist fast wie im Casino: Jedes Mal, wenn es einen Tag mit extremer Hitze gibt, passen sich Organismen mit einer gewissen Wahrscheinlichkeit an. Ob das nächstes Jahr passiert oder erst in zehn Jahren - wer weiß?“
Globalisierung schafft "Chancen" für pathogene Pilze
Dabei schafft die Globalisierung Gelegenheiten. Die Erfahrung mit dem Coronavirus und anderen neuen Erregern hat gezeigt: Je weiter wir in Ökosysteme vordringen, in denen potenzielle Krankheitserreger heimisch sind, umso wahrscheinlicher wird es, dass ein Erreger auf den Menschen überspringt. Das könnte auch für Pilze gelten, sagt Constantin Urban. "Ich glaube absolut, dass wir in der Zukunft mehr Pilzarten entdecken werden, die auch gesunde Menschen infizieren können und auch in diesen Menschen schwerere Infektionen auslösen können."
Und Arturo Casadevall betont: „Es steckt keine Intelligenz dahinter. So funktioniert Evolution nicht. Was passiert ist, dass wir Menschen dann ein Raum sind, in den die Pilze vordringen können.“
Ein erster tropischer Erreger hat es bereits geschafft, den Menschen hierzulande zu erschließen. Fusarium musae – ein Pilz, der eigentlich nur Bananen befällt. „Der führt dazu, dass Bananenbäume eingehen und dass die Bananen faulen", erläutert Oliver Kurzai, "und vor einigen Jahren wurde das erste Mal Fusarium musae auch von invasiven Infektionen isoliert. Da hat offensichtlich dieser Pilz, der sonst die Banane infiziert, es geschafft, auch den Menschen zu infizieren - und wir haben mittlerweile in Deutschland eine Handvoll Fälle, wo wir tatsächlich auch Fusarium musae als Erreger gefunden haben. Andere Länder haben das auch beschrieben. Die, ich sag mal, plausibelste Theorie - ohne dass das jemand jemals bewiesen hat – ist, dass dieser Pilz quasi mit dem Transport der Bananen aus Mittel und Südamerika in die deutschen Supermärkte tatsächlich dann auch hier eingeführt worden ist und dann hier – in zugegebener Weise sehr seltenen Fällen - Infektionen verursachen kann.“

Entwicklung neuer Antimykotika kompliziert
Noch sind es Einzelfälle, sagt Oliver Kurzai. „Pilze nutzen die Chance, aber die Zahl der Chancen nimmt durchaus zu.“ 1980 starben in den USA gerade einmal 800 Menschen im Krankenhaus durch invasive Pilzinfektionen. 20 Jahre später waren es schon 2.400, das Dreifache. Gleichzeitig sind Pilzinfektionen noch immer so selten, dass Ärzte und Ärztinnen kaum Erfahrung sammeln können. Dass die Infektionen auch in der Ausbildung kaum eine Rolle gespielt haben, könnte sich nun rächen.
„Es gibt mittlerweile gut dokumentiert mehrere Studien, die zeigen, dass schwere invasive Pilzinfektionen zu den am häufigsten übersehenen Krankheitsbildern auf Intensivstation zählen - auch und gerade in Europa, in den USA, also da, wo man denkt, man hat alles an Möglichkeiten. Das sind Erkrankungen, die schwer zu erkennen sind und deswegen auch häufig ganz übersehen oder zu spät erkannt werden.“
Die Auswahl an Medikamenten ist überschaubar. Was auch mit unserer evolutionären Nähe zu den Pilzen zu tun hat. „Viele Leute denken: Pilze sind so eine Art Pflanze ohne Grün, aber tatsächlich sind eigentlich Pilze eher Tiere ohne Bewegung. Diese enge Verwandtschaft führt dazu, dass es viel schwieriger ist, Medikamente zu entwickeln, die der Pilzzelle schaden, aber menschlichen Zellen nicht.“
Das macht die Entwicklung neuer Medikamente kompliziert. Unmöglich ist sie nicht. Kleinere Unternehmen haben in Antimykotika investiert und sind fündig geworden. „Wir haben aktuell eine Reihe von neuen Substanzen, darunter auch einige neue Substanzklassen in der klinischen Erprobung, die hoffentlich zeitnah - und zeitnah heißt wirklich in den nächsten drei Jahren - unser therapeutisches Spektrum erweitern werden", sagt Oliver Kurzai. "Das ist wirklich eine gute Nachricht. Trotzdem werden wir, auch wenn das alles klappt, immer noch weit weg sein von der Vielzahl der Antibiotika, die wir für die Behandlung von bakteriellen Infektionen haben.“
Killerpilz-Pandemie ist unwahrscheinlich
Die Welt wird sich weiter verändern und mit ihr die Pilze, von denen sich einige anpassen werden. Sie reisen um den Globus und treffen auf eine Bevölkerung, die älter und kränker wird. Wir sind nicht der bevorzugte Wirt der pathogenen Pilze, aber die Gleichgewichte verschieben sich.
„Wenn sie fragen: Müssen wir Angst haben, wir beide als gesunde Menschen, die keine schweren Grunderkrankungen haben? Da hoffe ich: Dann ist es sehr, sehr unwahrscheinlich, dass für uns Pilzinfektionen ein Problem werden. Deswegen müssen wir, glaube ich, nicht damit rechnen, dass wir in absehbarer Zeit tatsächlich, ich sag mal, eine Killerpilz-Pandemie kriegen, die auch den normalen gesunden Menschen bedroht.“